Белки и их функции. Свойства и функции белков
Среди органических веществ белки , или протеины , - самые многочисленные, наиболее разнообразные и имеющие первостепенное значение биополимеры. На их долю приходится 50 - 80% сухой массы клетки.
Молекулы белков имеют большие размеры, поэтому их называют макромолекулами . Кроме углерода , кислорода , водорода и азота , в состав белков могут входить сера, фосфор и железо. Белки отличаются друг от друга числом (от ста до нескольких тысяч), составом и последовательностью мономеров. Мономерами белков являются аминокислоты (рис. 1)
Бесконечное разнообразие белков создается за счет различного сочетания всего 20 аминокислот. Каждая аминокислота имеет свое название, особое строение и свойства. Их общую формулу можно представить в следующем виде:

Молекула аминокислоты состоит из двух одинаковых для всех аминокислот частей, одна из которых является аминогруппой (-NH 2 ) с основными свойствами, другая - карбоксильной группой (-COOH ) с кислотными свойствами. Часть молекулы, называемая радикалом (R ), у разных аминокислот имеет различное строение. Наличие в одной молекуле аминокислоты основной и кислотной групп обусловливает их высокую реакционную способность. через эти группы происходит соединение аминокислот при образовании белка. При этом возникает молекула воды, а освободившиеся электроны образуют пептидную связь. Поэтому белки называют полипептидами .
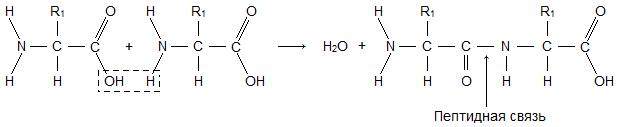
Молекулы белков могут иметь различные пространственные конфигурации, и в их строении различают четыре уровня структурной организации.
Последовательность аминокислот в составе полипептидной цепи представляет первичную структуру
белка. Она уникальна для любого белка и определяет его форму, свойства и функции.
Большинство белков имеют вид спирали в результате образования водородных связей между -CO-
и -NH-
группами разных аминокислотных остатков полипептидной цепи. Водородные связи малопрочные, но в комплексе они обеспечивают довольно прочную структуру. Эта спираль - вторичная структура
белка.
Третичная структура - трехмерная пространственная «упаковка» полипептидной цепи. В результате возникает причудливая, но для каждого белка специфическая конфигурация - глобула . Прочность третичной структуры обеспечивается разнообразными связями, возникающими между радикалами аминокислот.
Четвертичная структура
характерна не для всех белков. Она возникает в результате соединения нескольких макромолекул с третичной структурой в сложный комплекс. Например, гемоглобин крови человека представляет комплекс из четырех макромолекул белка.
Такая сложность структуры белковых молекул связана с разнообразием функций, свойственных этим биополимерам.
Нарушение природной структуры белка называют денатурацией
. Она может происходить под воздействием температуры, химических веществ, лучистой энергии и других факторов. При слабом воздействии распадается только четвертичная структура, при более сильном - третичная, а затем - вторичная, и белок остается в виде полипептидной цепи.
Этот процесс частично обратим: если не нарушена первичная структура, то денатурированный белок способен восстанавливать свою структуру. Отсюда следует, что все особенность строение макромолекулы белка определяются его первичной структурой.
Кроме простых белков , состоящих только из аминокислот, есть еще и сложные белки
Классификация белков. По форме молекул белки можно разделить на две большие группы – глобулярные (имеют сферическую форму) и фибриллярные (удлиненной формы). Так, глобулярными белками являются глобулины и альбумины крови, фибриноген, гемоглобин. Фибриллярные белки – кератин, коллаген, миозин и др. (рис.)
Белки, образованные только аминокислотами, называются простыми . Сложными являются белки, имеющие в своем составе компонент неаминокислотной природы. Это могут быть ионы металлов (Fe, Zn, Mg, Mn), липиды, нуклеотиды, сахара и др. Простыми белками являются сывороточный альбумин крови, фибрин, некоторые ферменты (трипсин) и др. Сложными белками являются липопротеины и гликопротеины (например, иммуноглобулины), а также большинство ферментов.
Денатурация и ренатурация белков . Одно из основных свойств белков - способность изменять свою структуру и свойства под влиянием различных факторов (действие концентрированных кислот и щелочей, высокая температура и др.). Процесс нарушения природной конформации белков под влиянием каких-либо факторов без нарушения первичной структуры называется денатурацией (от лат. де - приставка, означающая потерю, и натура - природные свойства) (рис.). Изменение структуры белка происходит вследствие разрыва водородных и ионных связей, стабилизирующих пространственные структуры. При денатурации могут утрачиваться четвертичная, третичная и даже вторичная структура. Денатурация сопровождается потерей биологической активности белка. При этом наблюдается уменьшение растворимости белка, изменение формы и размеров молекул, потеря ферментативной активности и т.д. Денатурирующими агентами являются: высокая температура, кислоты и щелочи, мочевина, спирты, фенол, хлорамин, соли тяжелых металлов и др. Так, соли тяжелых металлов (кадмия, ртути и др.) при взаимодействии с белками образуют нерастворимые соединения, и белки выпадают в осадок.
Как правило, денатурация имеет необратимый характер. Хотя на первых ее стадиях, при условии прекращения действия повреждающих факторов, белок может восстановить свое первоначальное состояние. Это явление называется ренатурацией (от лат. ре - приставка, обозначающая возобновление). В организмах обычно наблюдается частичная обратимая денатурация белков.
Способность белков к обратимому изменению своей структуры в ответ на действие физических и химических факторов лежит в основе важнейшего свойства всех живых систем - раздражимости .
Под влиянием некоторых факторов (воздействие формалина, спирта, щелочей и др.) может происходит разрушение первичной структуры. Процесс разрушения первичной структуры белков, называемый деструкцией (от лат. де - и структура - строение), всегда необратимый.
Явление денатурации часто используется в биологических исследованиях и в медицине. При определении в биологическом материале низкомолекулярных соединений из раствора сначала удаляют белки. Для этого вызывают их денатурацию, осаждают или отфильтровывают.
В медицине денатурирующие агенты часто применяются для стерилизации медицинских инструментов и материалов в автоклавах (здесь денатурирующий агент – высокая температура). Их используют также в качестве антисептиков (спирт, фенол, хлорамин и др.) для очистки загрязненных материалов и поверхностей. То же происходит при обеззараживании ран, ссадин, царапин раствором йода или спиртом. На денатурации белков основано применение мышьяковистого ангидрида в стоматологической практике при лечении пульпита.
Функции белков. Большое разнообразие белков позволяет им выполнять в живом организме множество различных функций, как структурных, так и метаболических.
Структурная. Белки входят в состав всех биологических мембран и органоидов клетки. Преимущественно из белков состоят хрящи, сухожилия. В их состав входит белок коллаген . Кератин – компонент перьев, волос, ногтей, когтей, рогов, копыт у высших животных. Эластин является компонентом связок, стенок кровеносных сосудов.
Каталитическая (ферментативная). Белковые молекулы ферментов способны ускорять течение биохимических реакций в клетках живых организмов в сотни миллионов раз. Ферменты участвуют как в процессах синтеза, так и распада веществ. Они обеспечивают расщепление питательных веществ в пищеварительном тракте, фиксацию углерода при фотосинтезе и т.д.
Механизм действия ферментов объясняет теория активного центра . Согласно ей, в молекуле каждого фермента имеется один или более участков, в которых происходит тесный контакт между молекулами фермента и специфического вещества - субстрата (рис.). Активным центром выступает функциональная группа (например, ОН-группа серина), отдельная аминокислота либо сочетание нескольких (в среднем от 3 до 12), расположенных в определенном порядке аминокислотных остатков. Форма и химическое строение активного центра таковы, что с ним могут связываться только определенные субстраты в силу точного соответствия их пространственных структур (как ключ и замок).
Молекула фермента вызывает ослабление определенных химических связей субстрата, и катализируемая реакция происходит с меньшими начальными затратами энергии, а следовательно, с намного большей скоростью. Ферменты ускоряют ход реакции без изменения ее общего результата за счет снижения энергии активации , т.е. в их присутствии затрачивается значительно меньше энергии для придания молекулам реакционной способности.
На заключительном этапе химической реакции фермент-субстратный комплекс распадается с образованием конечных продуктов и свободного фермента, который сохраняет исходную структуру и свойства. Освободившийся при этом активный центр может принимать следующие новые молекулы субстрата. Именно поэтому ферменты требуются в крайне низких концентрациях.
Некоторые ферменты, помимо активного центра, имеют один или несколько регуляторных центров. С этими участками могут связываться молекулы, регулирующие активность фермента. Они носят название активаторов (от лат. активус - деятельностный).
Молекулы некоторых веществ, взаимодействуя с ферментом, снижают или блокируют его активность (рис.). Такие вещества называются ингибиторами (от лат. ингибео – сдерживаю, останавливаю) . Например, многие лекарственные препараты природного или синтетического происхождения являются ингибиторами определенных ферментов. Кроме того, в основе действия некоторых токсических веществ лежит ингибирование активного центра ферментов.
Транспортная. Многие белки способны присоединять и переносить различные вещества. Гемоглобин связывает и переносит кислород и углекислый газ. Альбумины крови транспортируют жирные кислоты, глобулины - ионы металлов и гормоны. Молекулы белков, входящие в состав цитоплазматической мембраны, принимают участие в транспорте веществ в клетку и из нее.
Сократительная (или двигательная). Сократительные белки обеспечивают способность клеток, тканей, органов и целых организмов изменять форму, двигаться. Так, актин и миозин – обеспечивают работу мышц и немышечные внутриклеточные сокращения. Белок тубулин входит в состав микротрубочек веретена деления, ресничек и жгутиков эукариотических клеток.
Регуляторная . Некоторые пептиды и белки являются гормонами. Они влияют на различные физиологические процессы. Например, инсулин регулирует содержание глюкозы в крови. Глюкагон регулирует расщепление гликогена до глюкозы, повышая ее содержание в крови.
Сигнальная. Некоторые белки клеточных мембран способны изменять свою структуру в ответ на действие факторов внешней среды. Так происходит прием сигналов из внешней среды и передача информации в клетку. Примером может служить фитохром - светочувствительный белок, регулирующий фотопериодическую реакцию растений, и onсин - составная часть пигмента родопсина, находящегося в клетках сетчатки глаза.
Защитная. Специфические белки предохраняют организм от вторжения чужеродных организмов и от повреждений. Так в ответ на проникновение чужеродных тел - антигенов - в клетке вырабатываются антитела - особые белки, называемые иммуноглобулинами, которые обеспечивают иммунитет. Интерфероны защищают организм от вирусной инфекции. Фибриноген , тромбопластин и тромбин участвуют в свертывании крови и предотвращении кровопотери.
Токсическая. Многие живые существа в качестве собственной защиты выделяют белки, называемые токсинами , которые в большинстве случаев являются ядами для других организмов. Токсины синтезируются в организме некоторых змей, лягушек, насекомых, грибов, растений, бактерий. В свою очередь, некоторые организмы способны вырабатывать антитоксины , которые подавляют действие этих ядов.
Энергетическая. Белки могут служить источником энергии в клетке (после гидролиза). При полном окислении 1 г белка выделяется 17,6 кДж энергии. Белки расходуются на энергетические нужды в крайних случаях, когда исчерпаны запасы углеводов и жиров.
С белками могут взаимодействовать некоторые вещества и подавлять их функции. Такие вещества называются ингибиторами. Ингибиторами белковых функций являются многие яды. Так, например, ингибиторами белков-рецепторов постсинаптической мембраны, которые связываются с медиатором ацетилхолином при передаче нервного импульса в синапсах, являются мускарин (токсин мукора) и никотин . При этом нарушается проведение нервного импульса. Подобное действие оказывает также атропин – вещество, содержащееся в растениях красавки и белены. Атропин является ингибитором М-холинорецепторов. Учитывая, что связывание ацетилхолина с М-холинорецепторами вызывает сокращение многих гладких мышц, атропин используется как лекарственное средство, снимающее их спазм (спазмолитик). Однако при передозировке атропином могут наблюдаться двигательное и психическое возбуждение, галлюцинации, признаки понижения тонуса гладких мышц радужной оболочки глаз, бронхов, органов брюшной полости. Такой же эффект наблюдается при употреблении отваров белены (отсюда поговорка «белены объелся».
s1. Что общего и чем отличаются процессы денатурации и деструкции? 2. Чем обусловлено разнообразие свойств белков? 3 . Каковы основные биологические функции белков? 4. В чем состоит защитная функция белков? 5. Чем определяется двигательная функция белков? 6. Что такое ферменты? Почему без участия ферментов протекание большинства биохимических процессов в клетке было бы невозможным?
Среди органических веществ белки , или протеины , - самые многочисленные, наиболее разнообразные и имеющие первостепенное значение биополимеры. На их долю приходится 50 - 80% сухой массы клетки.
Молекулы белков имеют большие размеры, поэтому их называют макромолекулами . Кроме углерода, кислорода,водорода и азота, в состав белков могут входить сера, фосфор и железо. Белки отличаются друг от друга числом (от ста до нескольких тысяч), составом и последовательностью мономеров. Мономерами белков являются аминокислоты (рис. 1)
Бесконечное разнообразие белков создается за счет различного сочетания всего 20 аминокислот. Каждая аминокислота имеет свое название, особое строение и свойства. Их общую формулу можно представить в следующем виде:

Молекула аминокислоты состоит из двух одинаковых для всех аминокислот частей, одна из которых является аминогруппой (-NH 2 ) с основными свойствами, другая - карбоксильной группой (-COOH ) с кислотными свойствами. Часть молекулы, называемая радикалом (R ), у разных аминокислот имеет различное строение. Наличие в одной молекуле аминокислоты основной и кислотной групп обусловливает их высокую реакционную способность. через эти группы происходит соединение аминокислот при образовании белка. При этом возникает молекула воды, а освободившиеся электроны образуют пептидную связь. Поэтому белки называют полипептидами .

Молекулы белков могут иметь различные пространственные конфигурации, и в их строении различают четыре уровня структурной организации.
Последовательность аминокислот в составе полипептидной цепи представляет первичную структуру
белка. Она уникальна для любого белка и определяет его форму, свойства и функции.
Большинство белков имеют вид спирали в результате образования водородных связей между-CO-
и -NH-
группами разных аминокислотных остатков полипептидной цепи. Водородные связи малопрочные, но в комплексе они обеспечивают довольно прочную структуру. Эта спираль - вторичная структура
белка.
Третичная структура - трехмерная пространственная «упаковка» полипептидной цепи. В результате возникает причудливая, но для каждого белка специфическая конфигурация -глобула . Прочность третичной структуры обеспечивается разнообразными связями, возникающими между радикалами аминокислот.
Четвертичная структура
характерна не для всех белков. Она возникает в результате соединения нескольких макромолекул с третичной структурой в сложный комплекс. Например, гемоглобин крови человека представляет комплекс из четырех макромолекул белка.
Такая сложность структуры белковых молекул связана с разнообразием функций, свойственных этим биополимерам.
Нарушение природной структуры белка называют денатурацией
. Она может происходить под воздействием температуры, химических веществ, лучистой энергии и других факторов. При слабом воздействии распадается только четвертичная структура, при более сильном - третичная, а затем - вторичная, и белок остается в виде полипептидной цепи.
Этот процесс частично обратим: если не нарушена первичная структура, то денатурированный белок способен восстанавливать свою структуру. Отсюда следует, что все особенность строение макромолекулы белка определяются его первичной структурой.
Кроме простых белков , состоящих только из аминокислот, есть еще и сложные белки
Гидролиз белка
Любой белок состоит из аминокислот. Общая формула аминокислот есть 2HN-CHR-COOH. При образовании белка создаётся дипептидная связь:
2HN-CHR1-COOH + 2HN-CHR2-COOH -> 2HN-CHR1-CO-NH-CHR2-COOH + H2O.
Соответственно для гидролиза белка нужно разорвать дипептидную связь:
2HN-CHR1-CO-NH-CHR2-COOH + H2O -> 2HN-CHR1-COOH + 2HN-CHR2-COOH
Для определения белков среди других веществ используют качественные реакции:
а) Ксантопротеиновая реакция (б-к + HNO 3)
б) Биуретовая реакция (белок +Cu(OH) 2)
3. О п ы т. Как распознать с помощью характерной реакции соль серной кислоты среди трех выданных растворов солей?
ВЫПОЛНЕНИЕ:
Взять пробы из трех пробирок
Добавить в каждую пробу раствор хлорид бария, т.к. он является реактивом на сульфат ион
В пробирке с солью серной кислоты выпадает белый осадок сульфата бария
«Белки химия» - В состав слизи и синовиальной жидкости входят мукопротеиды. Структура белка. Кожа и волосы защищают внутреннюю среду организма от внешних воздействий. 2) Денатурация. Белки. Такие аминокислоты называются незаменимыми. Определение. Метионин лизин аргинин аспарагин аспарагиновая кислота глутаминовая кислота.
«Белка и Стрелка» - Белка и Стрелка первые космонавты. Стрелка в Музее Космонавтики. Через некоторое время у Стрелки появились щенки. Белка - беспородная самка белого окраса - была самая активная и общительная. Одними из наиболее приспособившихся собак-претендентов были Белка и Стрелка. 19 августа 1960 года был совершён успешный запуск космического корабля-спутника на орбиту.
«Урок Белки» - Конспект урока. Развивающая: развитие умения анализировать, сравнивать, делать выводы о свойствах белков. Белки. Уровни организации белковой молекулы. Рождение урока начинается: Почему молекулы аминокислот могут взаимодействовать между собой? Качественные реакции белков: биуретовая; ксантопротеиновая; реакция определения серы в белках.
«Дети с нарушением слуха» - Циолковский первым разработал модель ракеты, способной полететь в космос. Отставание мыслительной деятельности слабослышащих детей: С возникновением новых форм мышления старые формы не только не исчезают, а сохраняются и развиваются. Дети сравнительно поздно начинают осознавать свой дефект, как препятствие к развитию.
«Жиры белки углеводы» - Углеводы, как и жиры, являются энергетическим материалом. Что же такое рациональное питание? Проблема. Обед: макароны с сыром 430Ккал. Белки называют еще носителями жизни. Вывод. Результат. Наше питание. Задача. Узнать, почему необходимо правильно питаться и во время, чтобы не заболеть. От правильного питания будет зависить повышенность или пониженность нашего иммунитета.
«Белки урок» - Общие свойства белков. Структура белковой молекулы. Функции белков. Содержание белков в организме (в процентах к сухой массе). Качественные реакции. Что такое жизнь? Биуретовая Ксантопротеиновая HNO3 NaOH CuSO4. Белки. Содержание белков в пище. Четвертичная структура белковой молекулы.






